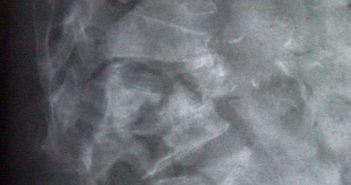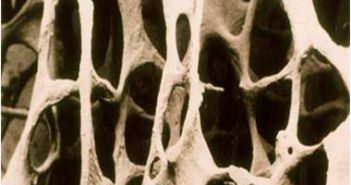
Comment prévenir l’ostéoporose et les chutes par l’activité physique en pratique ?
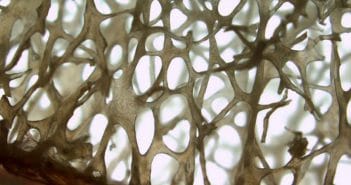
Certains programmes d’entraînement semblent avoir des effets bénéfiques sur le tissu osseux, notamment en réduisant significativement la perte osseuse post-ménopausique.
Les activités physiques en charge associées à des exercices de musculation et d’équilibre ont une action non seulement ostéogénique, mais peuvent agir sur les chutes et pourraient contribuer ainsi à réduire efficacement le risque de fracture. Néanmoins, les gains osseux apparaissent relativement limités et localisés au niveau des sites mécaniquement sollicités. De plus, il apparaît clairement que le maintien de l’entraînement est nécessaire à la conservation du gain osseux obtenu.
Les programmes d’entraînement proposés doivent nécessairement répondre à plusieurs contraintes, notamment être en adéquation avec les capacités physiques des sujets, mais également être relativement attractifs et peu contraignants, ce qui devrait augmenter leur adhérence.